医疗器械临床试验是基于“医疗器械临床试验质量管理规范”(行业也称医疗器械GCP)及相关法规开展的以验证医疗器械产品的安全性和有效性的研究活动。医疗器械临床试验主要包括临床试验准备阶段、临床试验实施阶段和临床试验结题阶段三个阶段,本文从医疗器械临床试验流程中各节点主要工作进行了解析。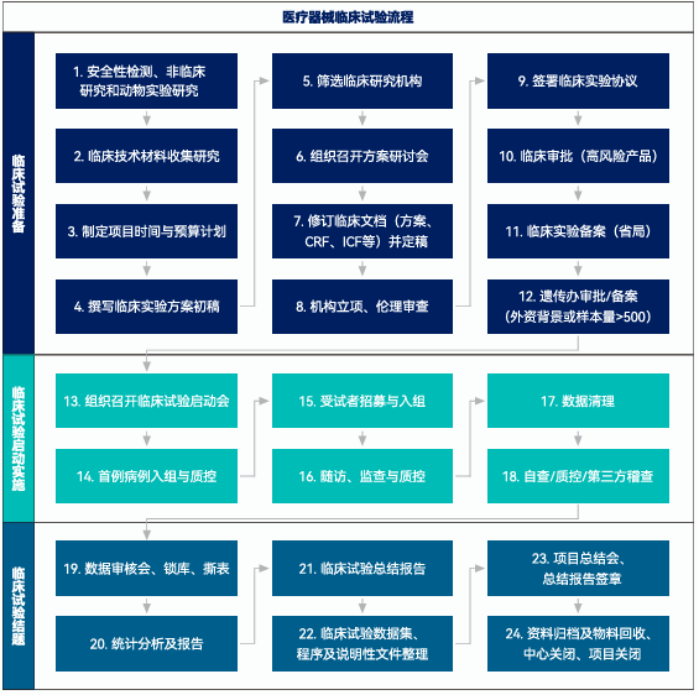
阶段一、临床试验准备
医疗器械临床试验前需先通过安全性验证,包括产品检测、动物实验及其它非临床研究。医疗器械临床试验应在已备案的医疗器械临床试验机构中开展。7.修订临床文档(方案、CRF、ICF、IB等)并定稿10.涉及高风险医疗器械,临床试验前应申请临床试验审批12.涉及外资背景的申办方或CRO或样本量大于500的还应申请人类遗传资源备案或审批22.临床试验递交数据整理,包括原始数据集、分析数据集、程序代码和说明性文件等
来源:公众号“CIRS医械合规动态”

